体内・細胞内動態特性の最適化を目指した
多機能性分子構造修飾型ワクチンの開発
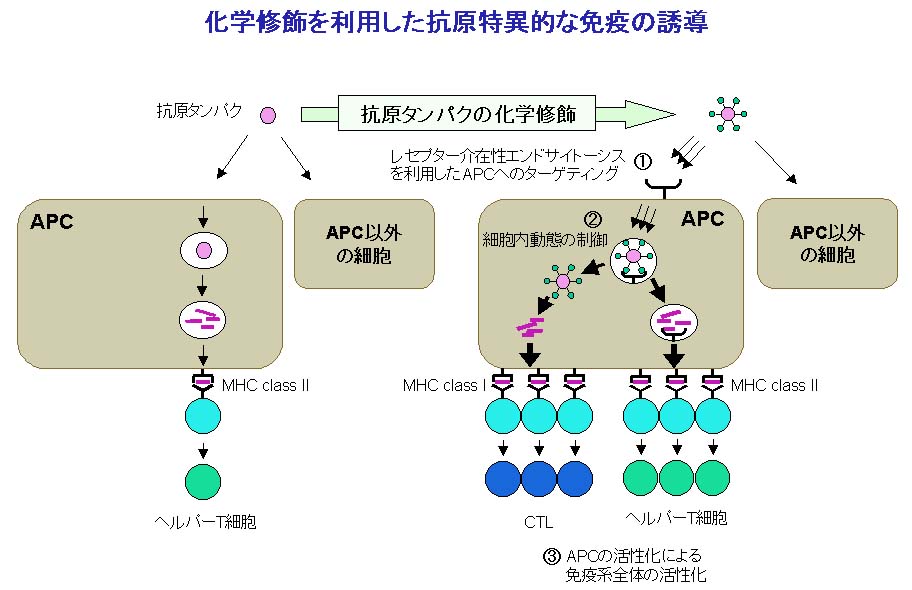
【研究の背景】
抗原特異的な免疫を誘導する免疫療法は、癌や感染症の有効かつ安全な治療法として期待されており、特に、細胞傷害性
T
リンパ球
(CTL)
を誘導することがこれらの疾病の治療に必要であると考えられています。
一般に
CTL
が誘導されるためには、マクロファージや樹状細胞などの抗原提示細胞
(APC)
が抗原タンパク質・抗原ペプチドを取り込んだ後、それを細胞内で分解し、生成されたペプチド断片を
MHC class I
分子上に提示する必要があります。より効率よく
CTL
を誘導させるため、これまで種々の方法が試みられてきましたが、従来の技術では十分な効果が得られていないのが現状です。その主な原因として、以下の
3
つが挙げられます。
(1)
抗原タンパク質・抗原ペプチドの
APC
への移行量自体が少ない。
(2) APC
に取り込まれた後の細胞内での抗原タンパク質・抗原ペプチドの動きが望ましくない。
(3) APC
の
CTL
誘導能が低いために、効率的な
CTL
の誘導が行われない。
【これまでの研究成果】
そこで、我々はこれらの問題点を克服し、効率的な
CTL
誘導が可能な新規ワクチンの開発に着手しました。
まず、
(1)
の問題を克服するには、抗原タンパク質・抗原ペプチドを効率よく
APC
に送り込む方法を確立しなくてはいけません。我々はその方法として標的である
APC
に発現しているレセプターに対して親和性を持つ分子(リガンド)を抗原タンパク質に化学的に結合させる方法を選択しました。負電荷を持つ高分子がスカベンジャーレセプターに取り込まれることに着目し、抗原タンパク質に負電荷を導入することで
APC
への効率よいデリバリーを図りました。まずワクチンの開発に先立ち、高分子のサイズや導入する負電荷の密度など、この機構を利用してタンパク質を
APC
に送り込むための合理的な設計の指針を確立しました
1)
。この情報を基に設計したワクチンは、効率よく抗原タンパク質を
APC
に送り込むことができることが確認され、その結果、効率よく
MHC class I
上に提示され、さらには特異的な
CTL
が誘導でき癌に対する生存日数の増大も確認できワクチンとして有用であることが明らかになりました
2-4)
。
一方で、電荷数を制御することで正電荷を有する抗原タンパク質を合成し、吸着性エンドサイトーシスにより
APC
に取り込ませることにより、
MHC class I
に抗原提示させることができ、その結果、
CTL
を効率よく誘導できることを明らかにしています
5)
。
さらに、近年、腫瘍免疫の分野において強力な免疫賦活化物質として注目されている
Heat Shock Protein
を利用したワクチンの開発にも取り組んでいます。
【参考文献】
-
Pharmacokinetic Analysis of In Vivo Disposition of Succinylated Proteins Targeted to Liver Non-parenchymal Cells via Scavenger Receptors: Importance of Molecular Size and Negative Charge Density for In Vivo Recognition by Receptors
Y. Yamasaki, K. Sumimoto, M. Nishikawa, F. Yamashita, K. Yamaoka, M. Hashida and Y. Takakura
J. Pharmacol. Exp. Ther. 2002 May;301 (2):467-477. Abstract (PubMed)- Efficient scavenger receptor-mediated hepatic targeting of proteins by introduction of negative charges on the proteins by aconitylation : the influence of charge density and size of the proteins molecules
Y. Yamasaki, J. Hisazumi, K. Yamaoka and Y. Takakura
Eur. J. Pharm. Shi. 2003 Apr;18 (5):305-12. Abstract (PubMed)- Disposition and Gene Expression Characteristics in Solid Tumors and Skeletal Muscle after Directe Injection of Naked Plasmid DNA in Mice
A. Kawase, T. Nomura, K. Yasuda, N. Kobayashi, M. Hashida and Y. Takakura
J. Pharm. Shi. 2003 Jun;92 (6):1295-304. Abstract (PubMed)- Efficient scavenger receptor-mediated uptake and cross-presentation of negatively charged soluble antigens by dendritic cells
K. Shakushiro, Y. Yamasaki, M. Nishikawa and Y. Takakura
Immunology. 2004 Jun;112 (2):211-8. Abstract (PubMed)- Induction of Cytotoxic T Lymphocytes following Immunization with Cationized Soluble Antigen
T. Ikenaga, Y. Yamasaki, K. Shakushiro, M. Nishikawa and Y. Takakura
Vaccine. 2004 Jun 30;22 (20):2609-16. Abstract (PubMed) - Efficient scavenger receptor-mediated hepatic targeting of proteins by introduction of negative charges on the proteins by aconitylation : the influence of charge density and size of the proteins molecules