Research
Total Synthesis of Zephycarinatines via Photocatalytic Reductive Radical ipso-Cyclization.
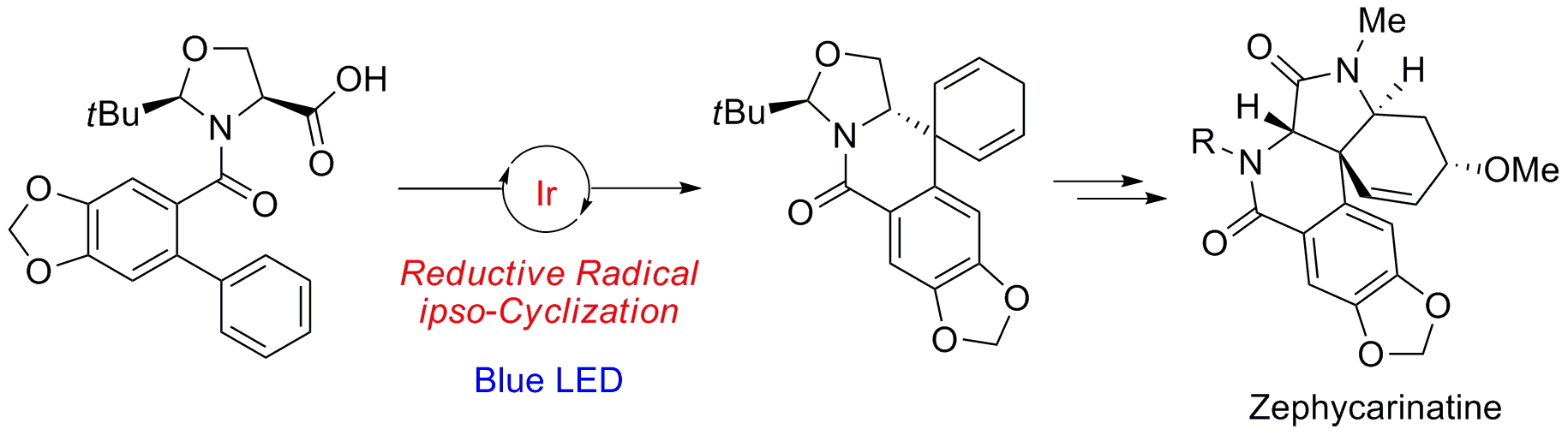
Zephycarinatineやzephygranditineは、ヒガンバナ科植物より単離されたアルカロイドであり、四級不斉炭素を含む複雑な五環性骨格を有する。これらのアルカロイドは、様々な腫瘍細胞株に対して増殖阻害活性を示すほか、NO産生阻害による抗炎症作用を示すことが報告されている。我々は、可視光レドックス触媒によるアミノ酸誘導体の脱炭酸を伴うラジカル生成と、それに続く分子内ipso環化反応を鍵反応としてzephycarinatine類の合成を計画した。t-Bu基をオキサゾリジン環上に有するカルボン酸に対して、Ir触媒存在下、青色LEDを照射すると、目的のスピロ体を単一のジアステレオマーとして得た。得られたスピロ体に対して種々変換を行うことによって、zephycarinatine CおよびDの全合成を達成した。さらに、本経路を用いて種々の誘導体を合成し、NO産生阻害活性を評価した。その結果、中程度の阻害活性を示す天然物誘導体を見出した。
Angew.Chem. Int. Ed.59(47)21210-21215. (2020)
Total Synthesis of (+)-Polyoxamic Acid via Visible-Light-Mediated Photocatalytic β-Scission and 1,5-Hydrogen Atom Transfer of Glucose Derivative.
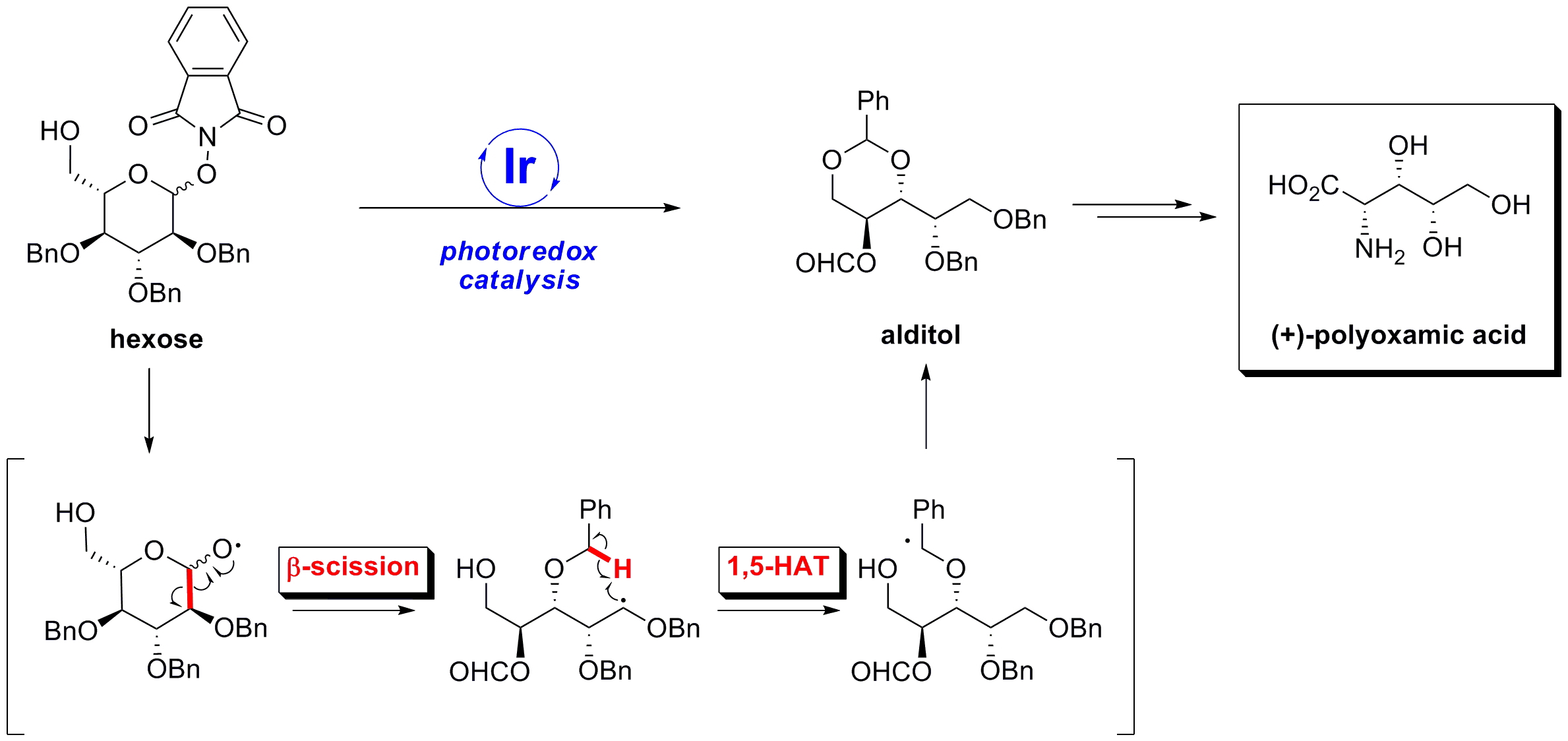
(+)-Polyoxamic acidは3つの連続不斉中心を有するαアミノ酸であり、polyoxinなどの生物活性天然物に含まれています。Polyoxinはペプチジルヌクレオシド系抗生物質であり、Candida albicansを含む多くの病原性真菌のキチンシンテターゼに対し活性を持つことが知られています。今回我々は、グルコースから容易に調製可能な化合物に対し、可視光レドックス触媒存在下、光照射を行うことによって、β開裂とC(sp3)-C(sp3) 1,5-HATが連続的に進行し、(+)-polyoxamic acidに誘導可能なアルジトールへ変換可能であることを見出しました。炭素ラジカルからの1,5-HATは、窒素ラジカルや酸素ラジカルを起点とした反応に比べ報告例が少なく、とりわけ、sp3炭素からの1,5-HATは、その安定化エネルギーの差が小さいゆえに特に困難とされています。さらに、本光反応をフロー反応へ適用し、(+)-polyoxamic acidの全合成を達成しました。
J. Org. Chem. 85(12) 8271-8278. (2020)
Construction of the pyrrolo[2,3-d]carbazole core of spiroindoline alkaloids by gold-catalyzed cascade cyclization of ynamide.
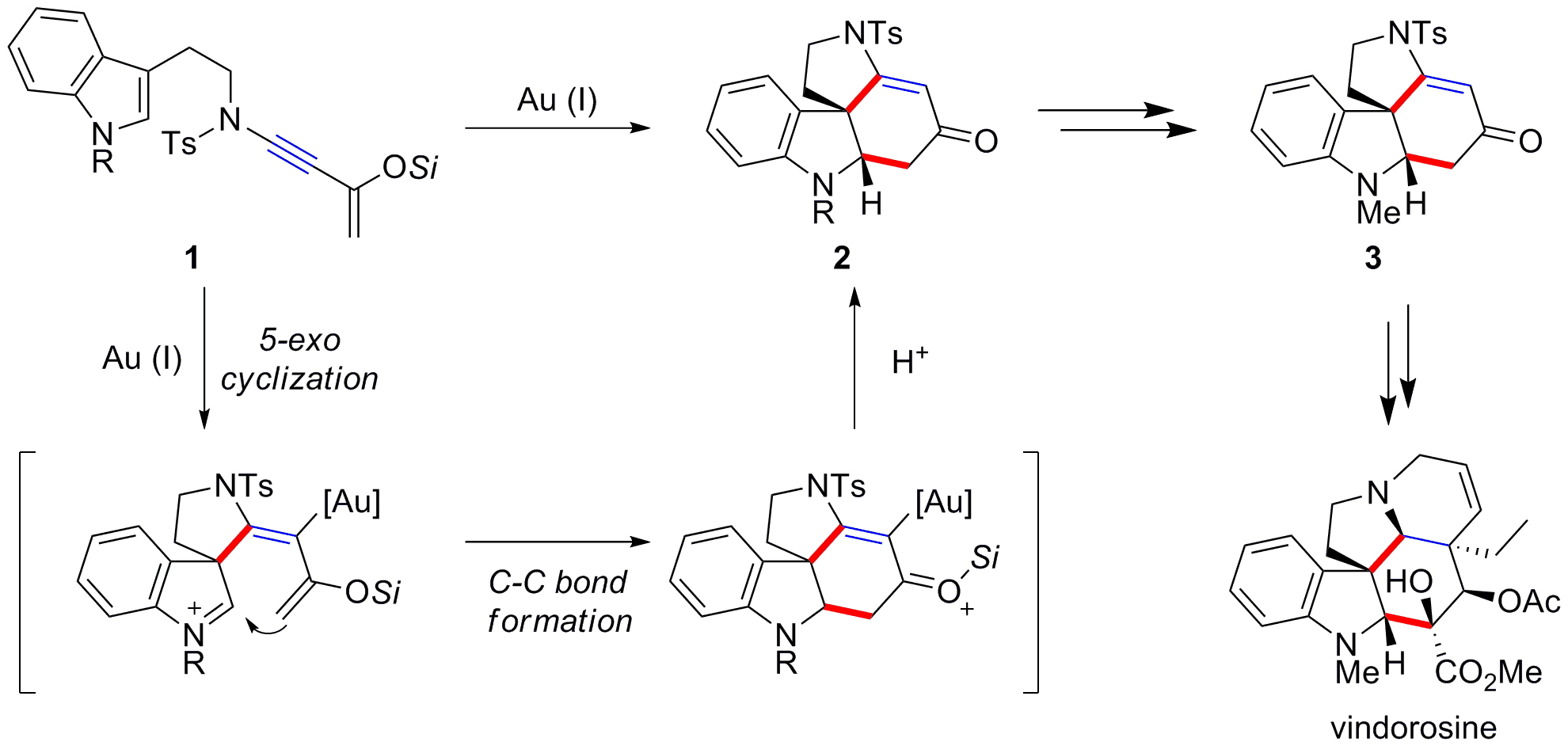
ピロロ[2,3-d]カルバゾールは、アスピドスペルマ型アルカロイドに広く見られる基本骨格です。そのため本骨格を効率的に構築する新規方法論は、関連するアルカロイド類の合成において有用な手法となります。今回我々は、シリルエノールエーテル部位を有するイナミド1に対し、金触媒を作用させることで、連続的に環化反応が進行し、ピロロ[2,3-d]カルバゾール2が得られることを見出しました。さらに、ピロロ[2,3-d]カルバゾール2の不斉合成と天然物合成への展開についても併せて検討を行い、光学活性なvindorosineの合成中間体へと導きました。
J. Org. Chem. 84(14) 9358–9363. (2019)
Construction of Quaternary Carbon Stereocenter of α-Tertiary Amine through Remote C–H Functionalization of Tris Derivatives: Enantioselective Total Synthesis of Myriocin.
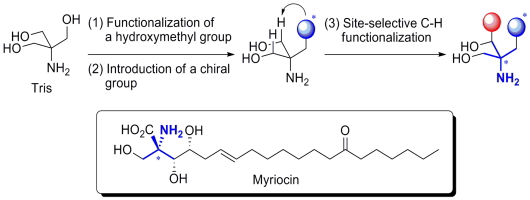
Myriocinは1972年に好熱菌から単離されたスフィンゴシン類縁体であり、強力な免疫抑制活性を示すことが知られている。構造的特徴としては、アミノ基が結合した不斉四置換炭素を含む3つの連続する不斉中心を有する。我々は安価で入手容易なTrisに着目し、Trisの3つの等価なヒドロキシメチル基を区別して官能基化することができれば、myriocinの不斉四置換炭素を構築可能であると考えた。すなわちTris中の任意の1つのヒドロキシメチル基を官能基化して不斉点を導入し、これを足掛かりとして、残る2つのヒドロキシメチル基の一方のC–H結合を選択的に官能基化することにより、望みの不斉炭素を構築することを計画した。Trisから容易に誘導可能な配座の固定されたアルコールを基質としたアルコキシラジカルを介する1,5-HAT反応を用いると、望みの選択的C–H結合官能基化反応が進行した。さらに種々の変換を行うことで、myriocinの全合成を達成した。
Org. Lett. 21(14) 5458–5490. (2019)
SAR study on odoamide: insights into the bioactivities of aurilide-family hybrid peptide-polyketides.
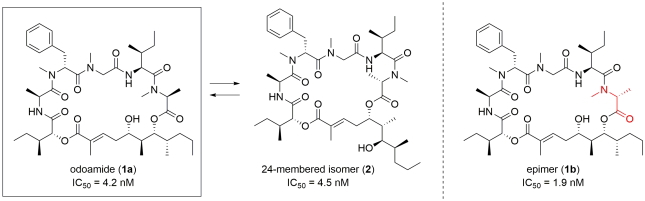
Odoamideは沖縄近海のシアノバクテリア類より単離された強力な細胞増殖抑制活性を示す環状デプシペプチドです。我々は、odoamideの活性に寄与する因子を明らかにすることを目的として、構造活性相関研究に取り組みました。まず、odoamide誘導体の効率的な合成経路を確立するとともに、複数の誘導体を合成し、天然物と同等の活性を有するペプチドを見出しました。また、天然物と24員環異性体が分子内アシル転位反応を介した平衡関係にあり、異性体も天然物と同等の生物活性を有することを明らかにしました。
ACS Med. Chem. Lett. 9(4) 365–369. (2018)
Total Synthesis and Stereochemical Revision of Stereocalpin A: Mirror-Image Approach for Stereochemical Assignments of the Peptide–Polyketide Macrocycle
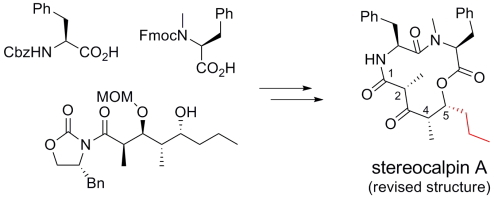
Stereocalpin Aは南極地方の地衣類より単離された細胞増殖抑制活性を示す環状デプシペプチドです。過去のstereocalpin Aの合成研究によりその提唱構造の誤りが指摘されており、現在まで天然物の立体化学は明らかではありませんでした。我々はstereocalpin Aの立体化学を決定することを目的として、合成研究に取り組みました。まず、stereocalpin Aのポリケチド部分の立体化学が異なる8種類の立体異性体を効率よく合成しました。得られた立体異性体と天然物とのNMRスペクトルの比較により、5位の立体化学が提唱構造とは異なる異性体のNMRスペクトルが天然物のものとよい一致を示しました。これにより、stereocalpin Aの全合成及び、構造修正を達成しました。
J. Org. Chem. 83(6) 3047-3060. (2018)
Total Synthesis of Dictyodendrins by the Gold-Catalyzed Cascade Cyclization of Conjugated Diynes with Pyrroles.
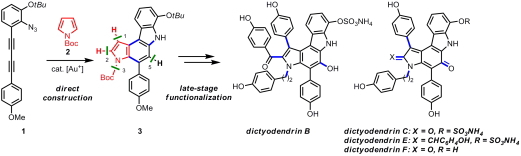
Dictyodendrin類は、海綿Dictyodendrilla verongiformisから単離されたインドールアルカロイドであり、高度に官能基化された四環性の基本骨格と、テロメラーゼ阻害等の魅力的な生物活性を有しています。本研究では、金触媒を用いた連続環化反応により一挙にDictyodendrin類の基本骨格を構築し、その後に置換基を導入する多様性志向型合成戦略を立案し、検討しました。その結果、金触媒存在下、共役ジイン1とピロール2を反応させることで、一挙にピロロカルバゾール3を得ることに成功しました。さらに、C1位、C2位、N3位、C5位を選択的に官能基化していくことで、Dictyodendrin B, C, E ,Fの合成を達成しました。
Angew. Chem. Int. Ed. 56(26) 7444-7448. (2017)
Total synthesis of odoamide, a novel cyclic depsipeptide from an Okinawan
marine cyanobacterium.
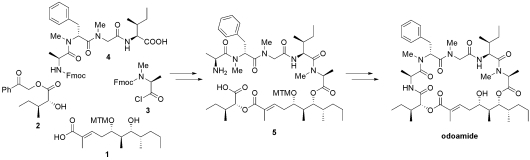
Odoamideは沖縄近海に生息するシアノバクテリア類より単離された、強力な細胞増殖抑制活性を有する環状デプシペプチドです。我々は、odoamideの絶対立体配置を明らかにすることを目的として、全合成研究を行いました。ポリケチド部分(1)の絶対立体配置を決定した後、各フラグメントを順次縮合し、odoamideの推定構造を合成しました。合成したodoamideの各種スペクトルデータは天然物とよい一致を示し、odoamideの初の全合成を達成しました。
Org. Biomol. Chem. 14(38) 9093-9104. (2016)
Total synthesis of (+)-conolidine by the gold(I)-catalyzed cascade cyclization
of a conjugated enyne
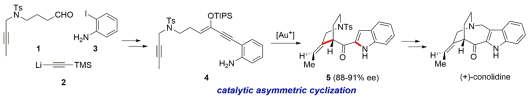
Conolidineは2004年にKamらによって単離されたアルカロイドであり、モルヒネなどとは異なるユニークな鎮痛活性を持つことが知られています。天然からの供給量が不十分であるため、創薬展開に適用できる効率的なconolidineの不斉合成法の開発が求められております。今回我々は、金触媒を用いた連続環化反応によるconolidineの不斉全合成を達成しました。我々の合成戦略は、共役エンイン4のエナンチオ選択的な金触媒連続環化反応により、conolidineの部分骨格であるインドール環とピペリジン環を一挙に構築できる点に特徴があります。本合成法は入手容易な前駆体1-3を用いた収束的な合成戦略を用いておりますので、関連化合物の多様性指向型合成法として有用であると考えています。
J. Org. Chem. 81(13) 5690-5698. (2016)
Novel 3,4,7-substituted benzofuran derivatives having binding affinity
to κ-opioid receptor
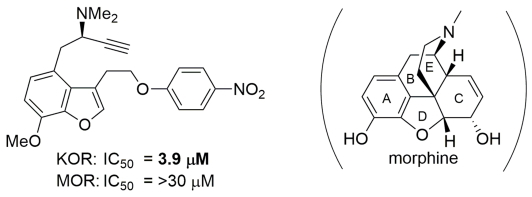
モルヒネに代表されるモルヒナンアルカロイドは、オピオイド受容体に作用して鎮痛作用をはじめとする様々な生物活性を示します。モルヒナン誘導体の使用においてしばしば問題となるのは依存の形成ですが、δ-
(DOR), κ- (KOR), μ-オピオイド受容体 (MOR) のうち、MORへの作用が依存の形成に関与していることが知られております。一方で、モルヒナン誘導体のC環部分の構造修飾は、受容体のサブタイプ選択性に大きく影響することも報告されています。我々は、C環部分の構造修飾を指向したモルヒナン誘導体の合成研究の過程において、いくつかの合成中間体がKORへの結合活性を有することを見出しました。興味深いことに、これらの誘導体はMORへの結合活性は示しませんでした。
Chem. Pharm. Bull. 64(7) 996-1003. (2016)
Formal total synthesis of (±)-strictamine based on a gold-catalyzed cyclization
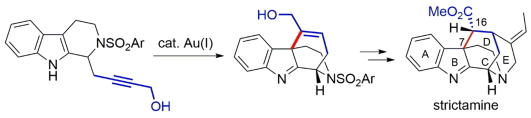
Strictamineは1966年にGanguliらにより単離されたモノテルペンインドールアルカロイドで、モノアミンオキシダーゼ阻害活性を有することが知られています。Strictamineの構造的特徴はA-E環からなる五環性カゴ型構造ですが、C7-C16位の結合形成による基本骨格構築は困難であることが知られていました。今回我々は、テトラヒドロ-β-カルボリン誘導体の金触媒環化反応を用いてD環を構築することに成功し、(±)-strictamineの形式全合成を達成しました。
Org Lett. 18(7) 1670-1673. (2016)
Synthesis and biological evaluation of the [D-MeAla11]-epimer of coibamide
A.
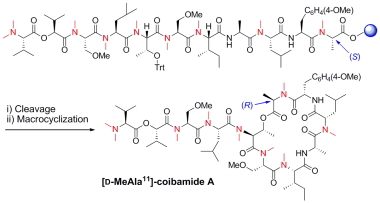
Coibamide Aは海洋シアノバクテリア類より単離された非常に強力な細胞増殖抑制活性を有する環状デプシペプチドです。我々は、各種縮合剤を用いたFmoc固相合成法とマクロラクトン化反応によるcoibamide
Aの合成を検討しました。マクロラクトン化反応において11位D-MeAlaのエピ体が得られたものの、本化合物は各種細胞株に対する細胞増殖抑制活性を示し、coibamide
Aをリードとする創薬研究のための有用な誘導体であることを明らかにしました。
Bioorg. Med. Chem. Lett. 25(2) 302-306. (2015)
Lewis-acid-mediated ring-exchange reaction of dihydrobenzofurans and its application to the formal total synthesis of (–)-quinocarcinamide
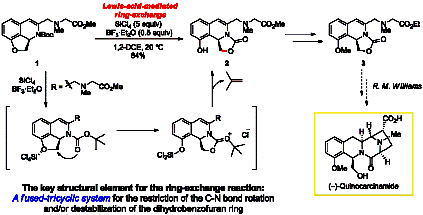
今回我々は、Boc 保護されたジヒドロイソキノリン1に対して、ルイス酸としてSiCl4とBF3・Et2Oを作用させると、室温化で速やかにオキサゾリジノン2が得られることを見出しました。本反応は、通常安定なジヒドロベンゾフランが温和な条件下開裂し、環交換生成物を与える点で興味深い反応です。種々のジヒドロベンゾフランを用いた検討により、縮環型三環性イソキノリン骨格が本環交換反応に必要な構造的要因であることを見出しました。また本反応を用いて、(–)-quinocarcinamideの形式不斉全合成を達成しました。
Tetrahedron Lett. 53(46) 6273-6276. (2012)
Total Synthesis of (-)-Quinocarcin by Gold(I)-Catalyzed Regioselective Hydroamination.
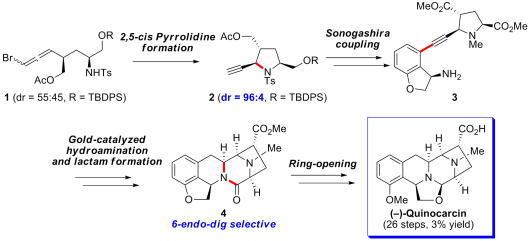
Quinocarcinは1983年に高橋と富田らにより単離されたテトラヒドロイソキノリンアルカロイドであり、リンパ性白血病細胞に対して高い増殖阻害活性を有する事が知られています。今回我々は、遷移金属触媒を用いた薗頭カップリング-環化反応によるquinocarcinの不斉全合成を達成しました。我々の合成戦略は (1) ブロモアレン1 のシス選択的分子内アミノ化反応による2,5-cisピロリジン2の合成、(2) 金触媒によるアルキン3の6-endo-dig選択的分子内ヒドロアミノ化反応、(3) ルイス酸を用いたジヒドロベンゾフラン4の開環反応を特徴としています。本合成法は、2つのユニットを合成終盤でカップリングさせる収束的な合成戦略を用いているため、関連アルカロイドの多様性指向型合成にも有用であると考えています。
Angew. Chem., Int. Ed.51(36) 9169-9172. (2012)
Pachastrissamine (jaspine B) and its stereoisomers inhibit sphingosine kinases and atypical protein kinase C.
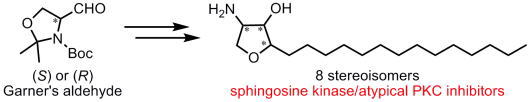
Pachastrissamineは、2002年に海洋生物pachastrissa sp. から単離された天然物であり、様々な腫瘍細胞株に対して細胞毒性を示すことが知られています。しかしながら、pachastrissamineの生物活性に寄与する標的分子に関する報告
例は数少なく、その効率的合成法の開発、構造活性相関研究や標的分子探索が精力的に行われています。我々は、これまでに確立した分岐的合成法により得られた
pachastrissamineの全立体異性体について、スフィンゴシンキナーゼ(SphK)およびプロテインキナーゼC(PKC)に対する阻害活性の評価を行い、全ての立体異性体がSphKおよびatypical
PKC阻害活性を示すことを明らかにしました。
Bioorg. Med. Chem. 19(18) 5402-5408. (2011)
Formal total synthesis of (+)-Lysergic acid via zinc(II)-mediated regioselective ring-opening reduction of 2-alkynyl-3-indolyloxirane.
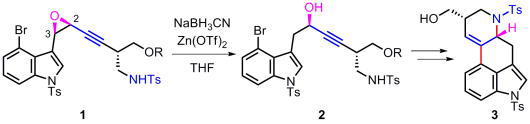
Ergot alkaloid類はカビの菌核より抽出されたインドールアルカロイドであり、リゼルグ酸をはじめとして数多くの天然物が報告されています。今回我々は、鍵反応であるルイス酸によるエポキシドの位置選択的開環反応を鍵反応とし
たリゼルグ酸の効率的な合成経路の確立を計画しました。収束的な経路により合成可能なアルキニルエポキシド1を用いて、種々の還元剤とルイス酸を検討した結果、亜鉛トリフレートとNaBH3CNを組み合わせた際に、目的のプ
ロパルギルアルコール2が選択的に得られることを見出しました。本反応においては、エポキシドへのルイス酸の配位と電子供与性のインドール環が協調的に作用して、位置選択的に3位が還元されたものと考えられます。続いて、当研
究室が開発したパラジウム触媒を用いたブロモアレンへの連続環化反応により、ergot alkaloid共通の四環性インドール骨格を有する3を得ました。得られた3はergot alkaloid共通の合成中間体であり、リゼルグ酸へは6工程で変換
可能です。このように我々は、ergot alkaloid類の新規合成経路の開発に成功しました。
J. Org. Chem. 76(13) 5506-5512. (2011)
Enantioselective total synthesis of (+)-Lysergic acid, (+)-Lysergol, and (+)-Isolysergol by palladium-catalyzed domino cyclization of allenes bearing amino and bromoindolyl groups.
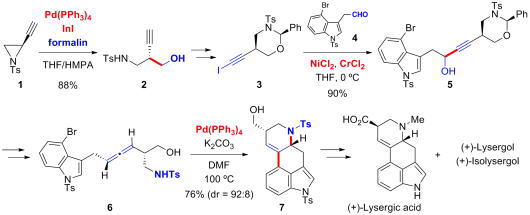
Ergot alkaloid類はカビの菌核より抽出されたインドールアルカロイドであり、リゼルグ酸をはじめとして数多くの天然物が報告されています。今回我々は、パラジウム触媒によるアレンの連
続環化反応を鍵反応としたergot alkaloid類の不斉全合成を計画しました。パラジウム触媒を用いたEthynylaziridine 1とホルムアルデヒドとの還元的カップリング反応により1,3-アミノアルコー
ル2を合成しました。2をヨード体3へと変換後、NHK反応を用いてアルデヒド4とのカップリング反応を行いました。得られたプロパルギルアルコール5をアレン6へと誘導し、パラジウム触媒による
連続環化反応によりergot alkaloid骨格を構築しました。さらに官能基変換により、(+)-lysergic acid, (+)-lysergol, (+)-isolysergolの不斉全合成を達成しました。
J. Org. Chem. 76(7) 2072-2083. (2011)
Ring-Construction/Stereoselective Functionalization Cascade: Total Synthesis of Pachastrissamine (Jaspine B) through Palladium-Catalyzed Bis-cyclization of Propargyl Chlorides and Carbonates.
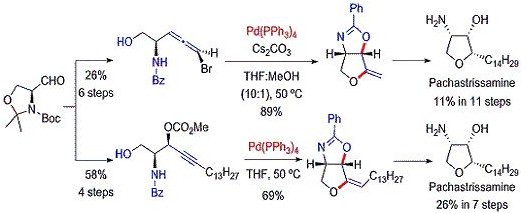
Pachastrissamineは沖縄近海に生息する海綿動物Pachastrissa sp. より抽出された天然物であり、様々な癌細胞株に対して細胞毒性を示すことが知られています。今回我々は、パラジウム触媒による
ブロモアレン及びプロパルギル化合物の連続環化反応を鍵反応としたpachastrissamineの全合成を計画しました。基質となるブロモアレン、プロパルギル化合物はGarner's aldehydeより合成しました。パラジウム
触媒を用いて検討を行ったところ、それぞれ良好な収率で、目的のテトラヒドロフラン環を構築することに成功し、pachastrissamineの全合成を達成しました。ブロモアレンを用いた経路では合成経路終盤に長鎖
アルキル基を導入するため、様々なアルキル基を有する誘導体の効率的な合成が可能です。一方、プロパルギル化合物を基質とした経路は短工程でpachastrissamineを与えます(7工程、26%)。また、パラ
ジウム触媒を用いたプロパルギル化合物の環化反応において、脱離基と求核部位の相対立体配置によって連続環化の反応性が異なることを明らかにしました。
J. Med. Chem. 75(11) 3831-3842. (2010)
Stereoselective divergent synthesis of four diastereomers of pachastrissamine (jaspine B).
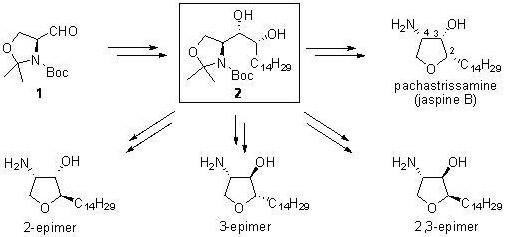
Pachastrissamineは2002年に沖縄近海に生息する海綿動物Pachastrissa sp.より抽出されたスフィンゴシン類縁体であり、様々な癌細胞株に対して細胞毒性を示すことが知られています。
今回我々は、pachastris¬samineに存在する3つの不斉中心の活性に対する影響を精査することを目的として、Garner’s aldehydeから2工程で得られるジオール2を共通の合成中間体として、4種類のジアステ
レオマーを分岐的かつ立体選択的に合成できる方法論を確立しました。
J. Org. Chem.753843-3846. (2010)
