
| TOP>融合研究コース 平成17年度 研究報告 | |
プロテアソーム阻害物質の合成と評価薬品分子化学分野 小林 裕輔 研 究 指 導 主 任 : 薬品分子化学分野 教授 竹本 佳司 研究指導協力者 : 生体機能解析学分野 教授 金子 周司 研究内容研究の背景と目的ユビキチンープロテアソームシステムは、選択的なタンパク質分解に重要な役割を果たしており、細胞周期、シグナル伝達、ストレス応答など多様な生命現象を制御するタンパク知るを特異的に分解し、それらの生命現象を調節している。あらたなプロテアソーム阻害物質は、さらなる生体内現象やタンパク質の機能解明ツールとして期待でき、さらには選択的、特異的な阻害様式によっては癌、炎症、免疫疾患などの治療薬としての応用も期待できるため、多くの注目を集めている。実際に、昨年、アメリカFDAによりプロテアソーム阻害物質PS-341(Velcade)が多発性骨髄腫の治療薬として認可されている。そこで、私は、近年単離された新規プロテアソーム阻害物質であるTMC-95AやSalinosporamideAに注目し、これらの類縁体合成を可能にする合成経路の開拓と研究過程で見出される新規化合物の活性評価実験を2研究室の融合研究として行い、活性構造相関を調べると共に、高活性な新規小分子のデザイン合成を行うことを計画した。 Proteasome Inhibitors; TMC-95A and Salinosporamide A
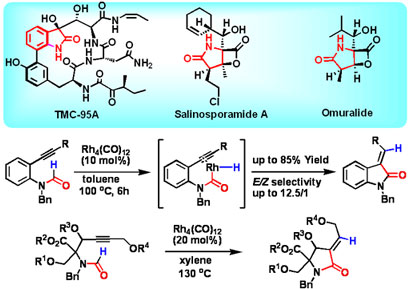 置換基によって活性の異なる化合物群の簡便合成法の開発を目指す 方法と期待される成果TMC-95Aは、これまでの共有結合形成によるプロテアソーム阻害物質と異なり、プロテアソームを阻害するのではなく、多点の水素結合を形成することで阻害活性を示すことが明らかとなり、多くの注目を集めている。本化合物を合成する際には、官能基化された環状構造を立体選択的に合成するかが鍵となる。そこで、我々は、容易に合成可能なホルムアミドのホルミルC-H結合を中性条件下、遷移金属触媒により活性化し、シス選択的にアルキンに挿入させて、E選択的に環状オレフィンを合成することを計画している。また、本反応(ヒドロアミド化反応)は官能基がまったく失われることがなく、有毒な一酸化炭素を用いなくてもカルボニル基を導入できる非常に効率的な反応であるが、これまで分子間のアルケンとの反応に限られており、分子内反応に成功すれば初めての報告例となる。 次に、本反応をSalinosporamideAの中心骨格である多置換ラクタム環の合成に展開することを計画している。SalinosporamideAは、深海の微生物Salinospora属の培養液から単離された [3.2.0] ビシクロβ-ラクトンγ-ラクタム構造をもつプロテアソーム阻害物質である。それ以前に発見された同じ骨格を持つOmuralideと置換基が異なるだけであるが、その35倍の阻害活性を示すため、そのプロテアソームに対する結合様式に興味がもたれており、プロテアソーム阻害機構の解明ため、様々な機関器を導入した縁類体を構築することを計画している。そこで、我々は、種々の天然アミノ酸から誘導した光学活性なアルキニルホルムアミドの分子内ヒドロアミド化反応を検討し、SalinosporamideAの中心骨格の簡便合成法を確立する。 Survey of Reaction Condition
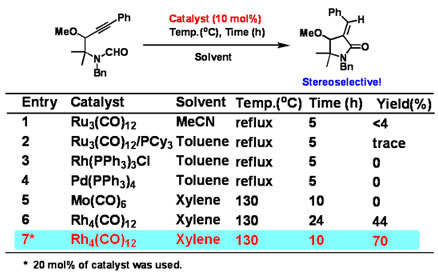 Application of various substrates
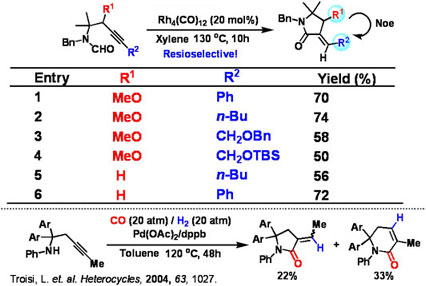 Application to Bi- and Tricyclic Compounds
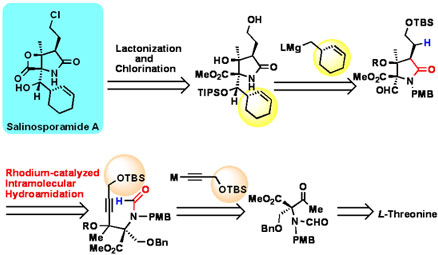
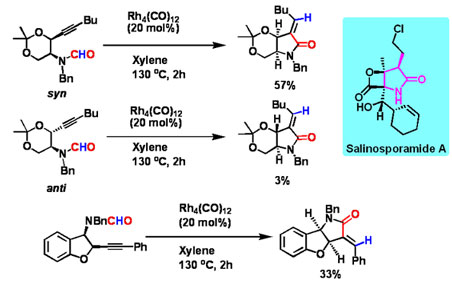 Retrosynthetic Analysis of Salinosporamide A
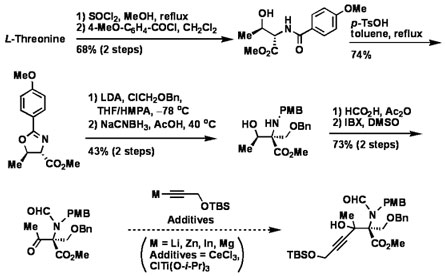
 Synthetic Root for Salinosporamide A (From L-Threonine)
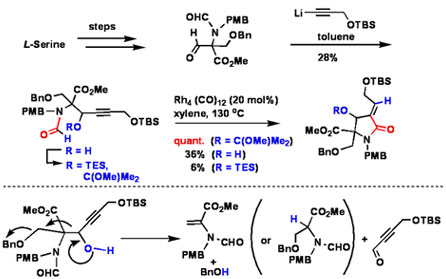
 Synthetic Root for Salinosporamide A (From L-Serine)
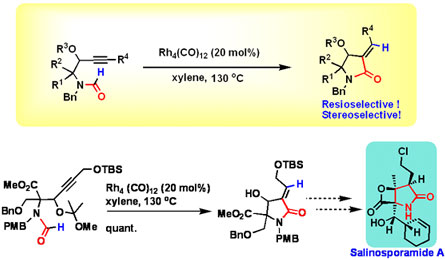
 Summary
 今後、開発した本手法により、まずSalinosparamide Aの全合成を目指す 天然物の中には、得意な薬理作用を融資、難病治療薬開発への応用がきたいできるものが多く存在する。しかし、多様な生理活性を併せもつ天然物においては、個々の活性の発現機構を明らかにしなければ実用化には程遠い。そのためには、まず目的の天然物を全合成し、類縁体合成を可能にする実用的な合成方法を確立する必要がある。本年度は、主に中心骨格の簡便合成法を確立することを計画しているが、今後は、合成研究を発展させて活性評価を行うための化合物ライブラリー構築を行う。本研究は、2研究室が融合し、プロテアソーム阻害物質の合成と活性評価を行う研究であり、活性効果を高めた新しい物質の創製だけでなく、生命現象の発現機構の解明への手助けとなると考えている。 |
|