心筋型リアノジン受容体の構造薬理学
2型リアノジン受容体(RyR2)は、心筋の筋小胞体に局在する超巨大な筋小胞体カルシウムイオンチャネルです(総分子量 ~2.2 MDa)。活動電位によって細胞外から流入したカルシウムイオンがRyR2に結合することでRyR2が開口し、筋小胞体に蓄えられたカルシウムイオンが瞬時に大量放出されることで心筋の収縮が引き起こされます。RyR2の先天性遺伝子変異(300箇所以上)は、カテコラミン誘発多形性心室頻拍(CPVT)等の致死的な不整脈疾患の原因としても知られており、RyR2は不整脈疾患の標的分子としても注目を集めています(J Muscle Res Cell Motil, 2020)。
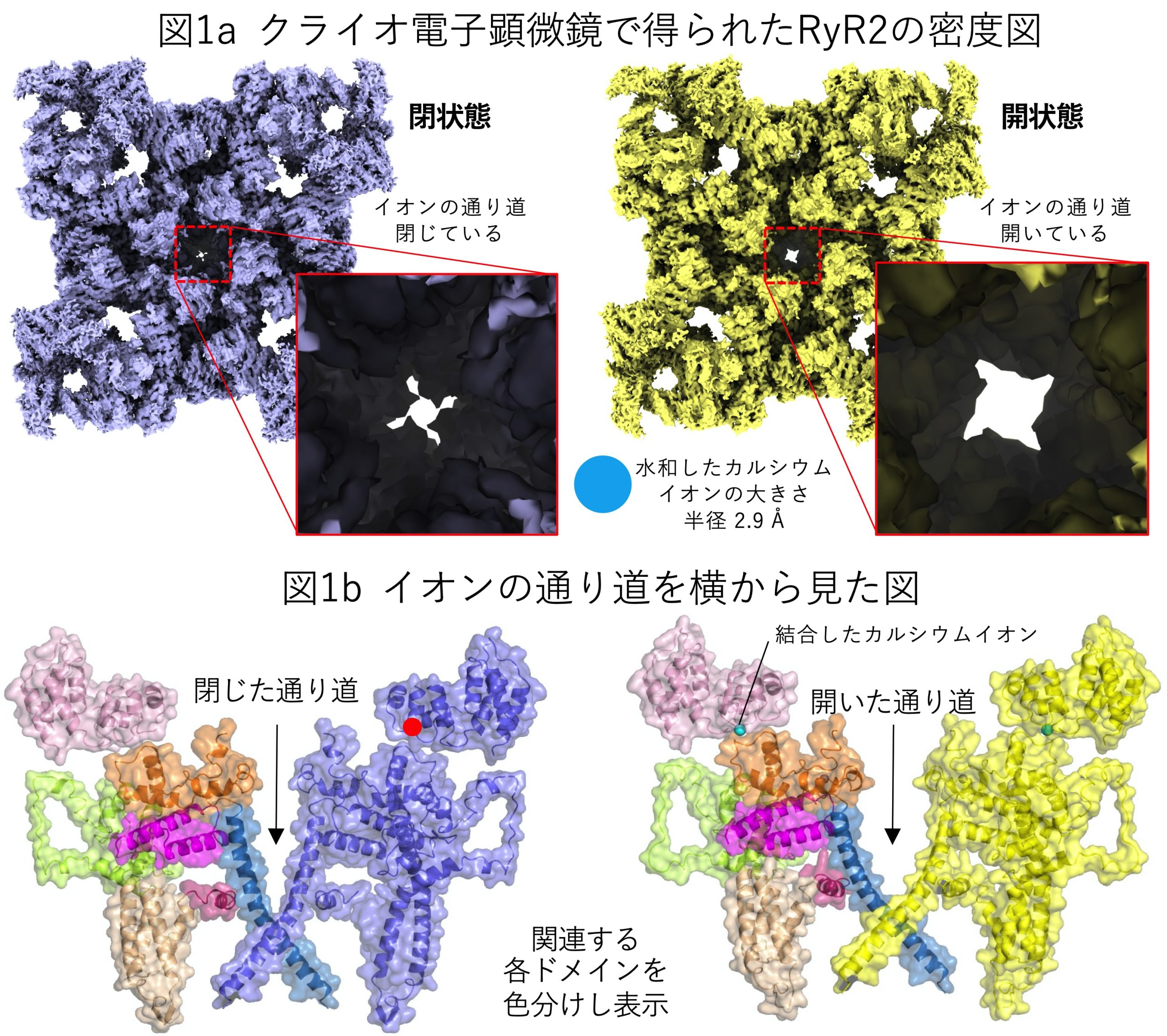
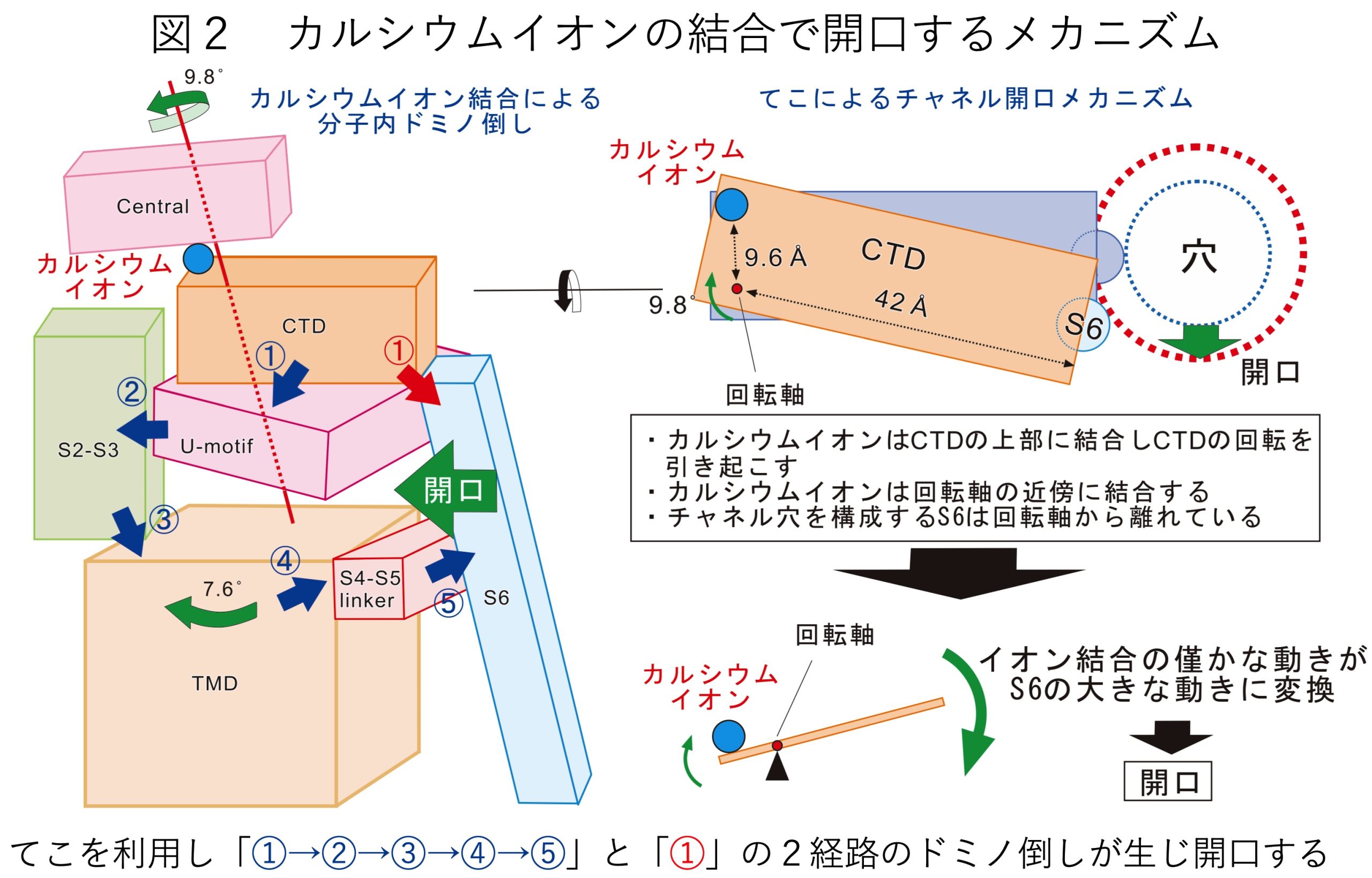
このRyR2はたった4つのカルシウムイオンが結合することで開口することが知られていましたが、カルシウムイオンのような小さな分子が、一体どのようにして自身の6万倍もの大きさを持つ超巨大分子RyR2を制御し、イオンを通す孔を開くのでしょうか?科学的にも医学的にも大変興味深い問いかと思います。私たちは、この50年来の謎に対し、クライオ電子顕微鏡を武器に、チャネルが「閉じた」状態と「開いた」状態の精密な立体構造の解明に至りました(図1, Nat Commun, 2022)。RyR2は17個ものドメインから構成されますが、詳細な機能解析実験と組み合わせることで、これらのドメインが「ドミノ倒し」をするように次々と動くことが判明しました(図2左)。また、要所要所にはドミノ倒しが自然に起こらないようなストッパーが存在することも予測されました。さらに、カルシウムイオンはCTDドメインの左端近傍に結合し、それに伴いCTDが時計回りの回転運動を起こすことも明らかになりました(図2右)。回転軸はカルシウムイオン結合部位のごく近傍にあり、イオンの通り道を制御するS6ドメインは回転軸から遠く離れたCTDの右端に接続していることから、カルシウムイオン結合部位での僅かな動きが「てこ」の原理によりS6での大きな動きへと変換されることがわかりました(図2右)。
現在は、RyR2疾患変異体がチャネル開口の異常を引き起こす機構、CPVTの効果的治療薬として開発を進めている合成化合物(Kurebayashi et al., in press)がRyR2を調節する機構、RyR2の調節因子として機能するカルモジュリン等との複合体構造、さらに脂質との相互作用などについて研究を進めております。
Ogawa H., Kurebayashi N., Yamazawa T., Murayama T.
Regulatory mechanisms of ryanodine receptor/Ca2+ release channel revealed by recent advancements in structural studies.
J Muscle Res Cell Motil, 42, 291-304, 2020.
Kobayashi T., Tsutsumi A., Kurebayashi N., Saito K., Kodama M., Sakurai T., Kikkawa M., Murayama T., Ogawa H.
Molecular basis for gating of cardiac ryanodine receptor explains the mechanisms for gain- and loss-of function mutations.
Nat Commun, 13, 2821, 2022.
Kurebayashi N., Kodama M., Inoue H., Konishi M., Sugihara M., Murayama T., Ishida R., Ishii K., Mori S., Endo Y., Zeng X., Inoue Y. U., Inoue T., Noguchi S., Nishio H., Nakashima E., Suzuki N., Nakaya N., Sato R., Otori Y., Tsutsumi A., Takahashi M., Oka T., Ogawa H., Kanamitsu K., Kusuhara H., Yokoyama U., Kurokawa J., Kagechika H., Sakurai T.
A novel RyR2-selective stabilizer prevents stress-induced ventricular arrhythmias without impairing cardiac function.
Br. J. Pharmacol. in press
