低酸素誘導因子存在領域を検出するための放射性プローブ開発
低酸素誘導因子存在領域を検出するための放射性プローブ開発
固形腫瘍には、細胞増殖に対して血管からの酸素供給が追いつかない低酸素領域が存在する。この領域では低酸素誘導因子(HIF-1)が発現しており、血管新生、浸潤・転移に関与するタンパク質発現を亢進させることで、腫瘍の悪性化、治療抵抗性につながることが知られている。従って、腫瘍内のHIF-1発現を非侵襲的にイメージングできれば、腫瘍の性状把握・質的診断、治療計画策定に有用であると考えられる。
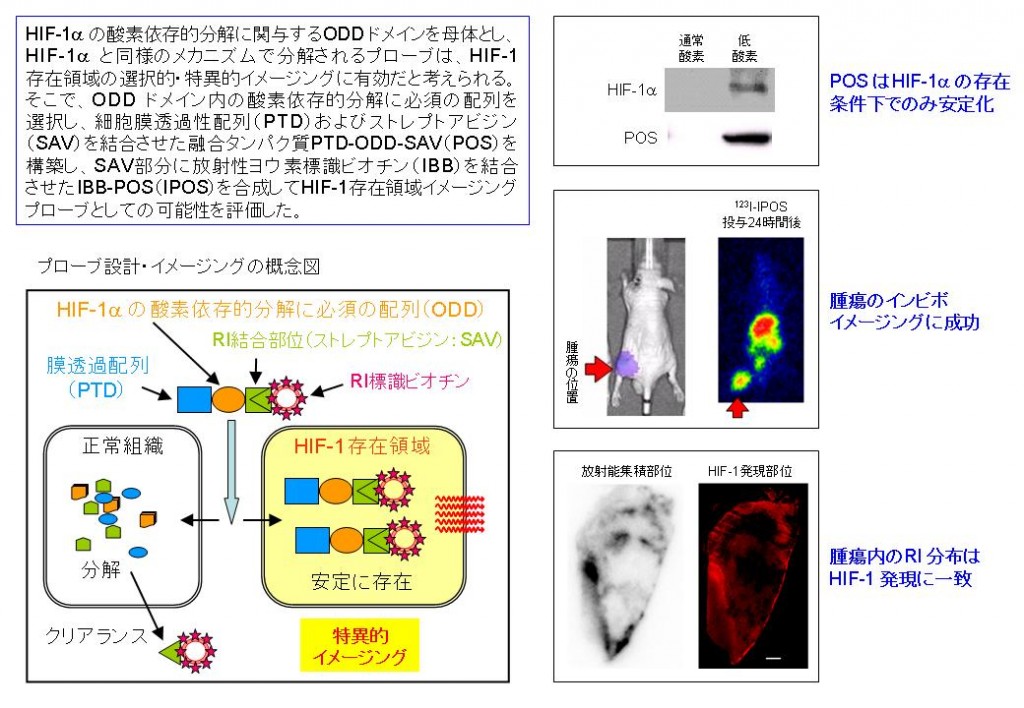
HIF-1はαとβの2種類のサブユニットからなり、その活性は酸素依存的に分解されるαサブユニットの量によって調節されている。すなわち、HIF-1αの酸素依存的分解に関与するペプチド配列を母体とし、HIF-1αと同様のメカニズムで酸素依存的分解を受けるプローブを開発すれば、腫瘍内のHIF-1存在の有無が非侵襲的に検出可能になると考えられる。
この概念に基づき、融合タンパク質プローブ123I-IPOSを開発してその評価を行ったところ、所期の通りHIF-1αの存在する条件下でのみ安定に存在し、通常酸素条件下ではプローブ全体が分解されることが確認できた。さらに123I-IPOSはインビボで腫瘍集積性を示し、その腫瘍内分布はHIF-1α存在領域に一致することを認めた。
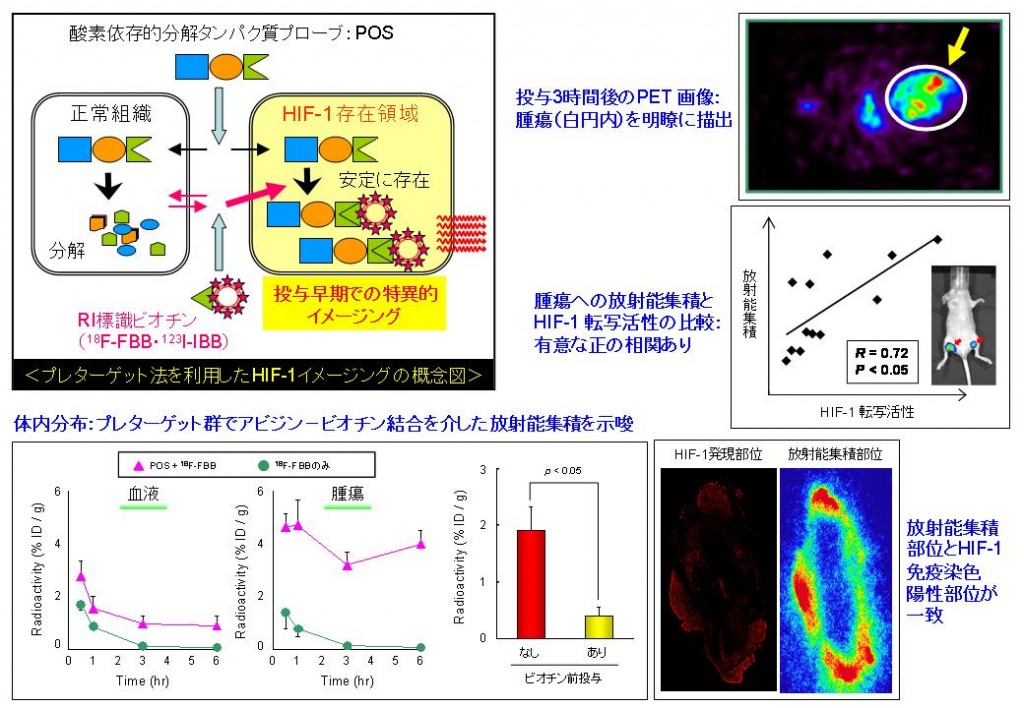
次に、融合タンパク質の血液クリアランスの遅さを克服し、RIプローブ投与早期から高コントラスト画像を得るために、まずPOSのみを投与(プレターゲット)し、正常組織での分解・クリアランス及びHIF-1存在領域での滞留が達成されたあとに、POSとの結合性を有する低分子RIプローブを投与してインビボでPOSとカップリングさせるプレターゲット法の有効性について検討した。
アビジン-ビオチンの高親和性結合に着目し、低分子RIプローブとして放射性フッ素あるいは放射性ヨウ素標識ビオチン誘導体(18F-FBB,123/125I-IBB)を設計・合成して利用したところ、POSをプレターゲットされた場合にのみ腫瘍への顕著な放射能集積を認めた。この集積は過剰量のビオチン前投与によって阻害された。さらに、18F-FBBを用いた場合は投与早期(3時間後)から明瞭に腫瘍をイメージングすることが出来、その集積量・腫瘍内局在はHIF-1転写活性・存在領域と相関した。これらの結果から、POSのプレターゲットとそれに結合する放射性ビオチン誘導体を用いることで、腫瘍内HIF-1存在領域の投与早期イメージングが可能となることが明らかとなった。
主要論文
- Development of an Oxygen-Sensitive Degradable Peptide Probe for the Imaging of Hypoxia-Inducible Factor-1-Active Regions in Tumors
Mol. Imaging Biol. 15 (6) 713-721 (2013) - Evaluation of [125I]IPOS as a molecular imaging probe for hypoxia-inducible factor-1-active regions in a tumor: Comparison among single-photon emission computed tomography/X-ray computed tomography imaging, autoradiography, and immunohistochemistry.
Cancer Sci. 102 (11) 2090-2096 (2011) - PET imaging of hypoxia-inducible factor-1-active tumor cells with pretargeted oxygen-dependent degradable streptavidin and a novel 18F-labeled biotin derivative.
Mol. Imaging Biol. 13 (5) 1003-1010 (2011) - Rapid detection of hypoxia-inducible factor-1-active tumours: pretargeted imaging with a protein degrading in a mechanism similar to hypoxia-inducible factor-1alpha.
Eur. J. Nucl. Med. Mol. Imaging 37 (8) 1566-1574 (2010) - Imaging of HIF-1-active tumor hypoxia using a protein effectively delivered to and specifically stabilized in HIF-1-active tumor cells.
J. Nucl. Med. 50 (6) 942-949 (2009)